การจัดเรียงอิเล็กตรอน(electron configuration)
🐙ระดับพลังงานหลัก (shell)
n คือระดับพลังงานหลัก(principal energy level) หรือเชลล์(shell) ซึ่งเป็นเลขจำนวนเต็มหลักการ
อิเล็กตรอนมากสุดในแต่ละดับชั้นพลังงาน = 2n^2(n คือระดับชั้นพลังงาน)
n = 1 ⇨ K 💨 2
n = 2 ⇨ L 💨 8
n = 3 ⇨ M 💨18
n = 4 ⇨ N 💨 32
n = 5 ⇨ O 💨 50
n = 6 ⇨ P 💨 72
n = 7 ⇨ Q 💨 98

🐙ระดับพลังงานย่อย (sub shell)
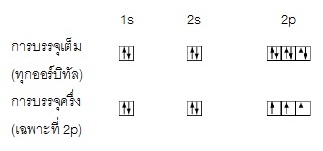
แบ่งออกเป็นดังนี้🌳s มี 1 ออร์บิทัล มีจำนวนอิเล็กตรอนทั้งหมด 2 ตัว
🌳p มี 3 ออร์บิทัล มีจำนวนอิเล็กตรอนทั้งหมด 6 ตัว
🌳d มี 5 ออร์บิทัล มีจำนวนอิเล็กตรอนทั้งหมด 10 ตัว
🌳f มี 7 ออร์บิทัล มีจำนวนอิเล็กตรอนทั้งหมด 14 ตัว


(4).jpg)

ไม่มีความคิดเห็น:
แสดงความคิดเห็น